칼피셔법과 수분 측정 3가지 방법
칼피셔법과 수분 측정 3가지 방법
칼피셔법과 실험실에서 수분 측정 시 사용하는 3가지 방법을 알아보겠습니다.
칼 피셔법(Karl-Fischer method)
칼 피셔법(Karl Fischer Titration)은 시료 내의 수분(물) 함량을 정확하게 측정하기 위한 화학적 분석 방법입니다. 이 방법은 매우 정밀하고 광범위하게 사용되며, 특히 제약, 화학, 식품, 석유 등의 산업에서 수분 측정에 많이 사용됩니다.
KF 또는 칼피셔 적정법은 샘플에서 미량의 물을 결정하기 위한 고전적인 적정 기술 중 하나로 1935년 독일 화학자 칼 피셔에 의해 처음 발명되었습니다. 이때 사용하는 요오드시약을 독일 화학자 이름을 따서 칼 피셔(Karl-Fischer) 시약이라 합니다. 보통 이 방법은 자동화된 칼 피셔 적정기를 사용하여 수행되며 아래 용량적정법과 전량적정법에서 사용합니다.
칼피셔 시약은 요오드, 이산화황 및 피리딘 등을 무수메탄올 용액으로 하여 만들어집니다. 수분을 측정 시에는 요오드와 이산화황 사이에 산화환원반응(요오드로 이산화황을 산화시키는데 요오드로 물의 몰 당량 1개만 소모)으로 수분과 반응하게 되는데 반응 후 당량점을 지나면 요오드가 과잉하게 되고 그것을 검출함으로써 종점을 구할 수 있습니다.
- I2(요오드): 반응을 통해 물을 산화하는 역할
- SO2(이산화황): 물과 반응해 적정이 가능한 화합물을 생성
- C5H5N(피리딘): 촉매 역할을 하고, 반응이 진행되도록 돕는 역할
육안으로 봤을 때 칼피셔 시약은 요오드가 들어가 있어 짙은 보라색을 나타냅니다. 검체를 녹이는 용매는 칼피셔 용액으로 수분을 제거하면서 요오드로 인해 약간의 보라색을 띱니다.
용매에 검체(수분)가 들어가면 투명하고 맑은 액이 되고 적정을 시작하면 칼 피셔시약이 들어가면서 당량점에 이를 경우 짙은 보라색이 나타냅니다.
1. 용량적정법(Volumetric)
용량적정법은 칼피셔시약을 검체를 녹일 수분측정용 시액에 녹여 수분을 제거하고, 검체의 물과 반응하여 소비된 칼피셔시약 적정량(용량)으로부터 수분을 측정하는 방법입니다. 적정의 종말점은 전극을 통해 검출하며 소비된 칼피셔 시약의 용량으로 수분을 측정하기 때문에 수분과 반응하는 칼피셔 시약의 Titer 값이 중요한 Factor입니다. 가장 대중적으로 사용하는 시험방법입니다.

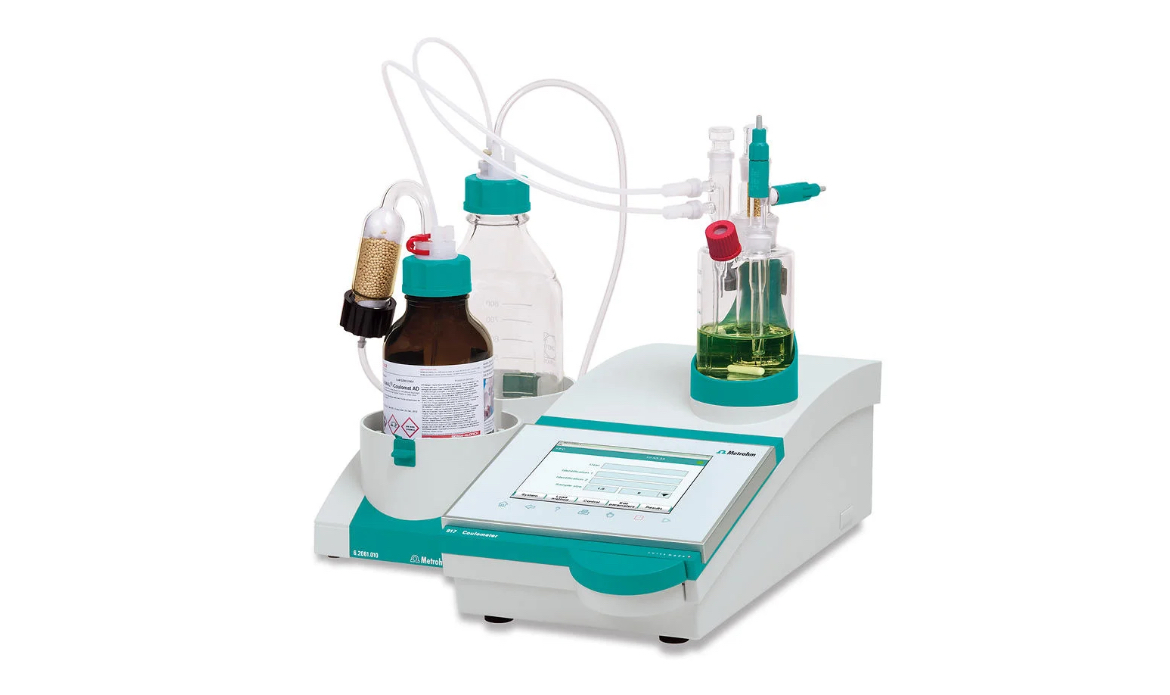
2. 전량적정법(Coulometric)
전량적정법은 전기전하량(C/쿨롱)을 통해 미량의 수분을 측정하는 방법입니다. Generator 전극에서 요오드(I2)를 생성시켜 물과 반응시켜 분석하기 때문에 Karl Fischer 시약의 Titer를 따로 측정할 필요가 없습니다. 주로 0.1% 이하 (1,000ppm 이하)의 미량 수분 측정에 적합한 시험방법입니다.
3. 할로겐 수분측정법
할로겐 수분 측정법은 할로겐램프를 사용하여 검체를 가열하고 감량된 무게로 수분량을 결정하는 수분 분석방법입니다. 기기 자체로 검체의 무게를 측정하고 적외선 방사기(할로겐램프)로 가열하며 정의된 기준에 도달할 때까지 중량 손실을 시간 간격을 설정하여 지속적으로 기록합니다. 검체에 수분 외에 다른 요소(잔류용매 등)를 감안하지 않을 때 사용할 수 있으며 다른 검체의 칭량 및 할로겐 가열 장비로 구성됩니다.

실험실에서는 위의 3가지 방법을 대중적으로 사용하고 있습니다. 일반적으로는 용량적정법, 미세한 수분측정에는 전량적정법, 간단하게 건조량으로 수분을 측정하고 싶을 때는 할로겐 수분측정법을 사용하고 있죠. 실험실에서 필요한 용도에 따라서 위 3가지 시험방법을 고려하여 이용한다면 좀 더 효율적으로 검체의 수분을 측정할 수 있을 겁니다.