아질산염(Nitrite)의 정의와 특성, 니트로사민과의 연관성을 알아보자
1. 정의
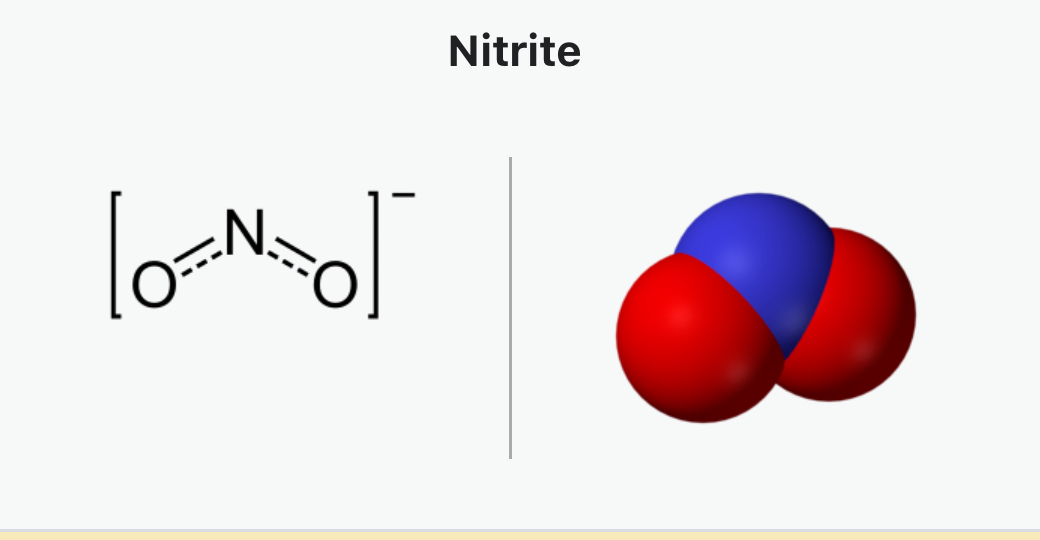
아질산염(nitrite)은 질소 원자와 산소 원자가 결합한 화합물로, 화학식은 NO₂⁻입니다. 이는 질산염(nitrate, NO₃⁻)과 구분되며, 산화 상태에서 질소의 산화수가 +3인 상태를 나타냅니다. 아질산염은 자연계와 산업에서 다양한 형태로 존재하며, 화학적, 생물학적 특성 때문에 여러 용도로 사용됩니다.
2. 특성
- 화학적 특성
구조(Structure) : 아질산염 이온은 공명 구조를 가지며, 질소 원자에 두 개의 산소 원자가 결합되어 있습니다. 한 산소는 단일 결합, 다른 하나는 이중 결합으로 나타나지만, 실제로는 전자가 비편재화되어 두 결합이 동일한 성격을 띱니다.
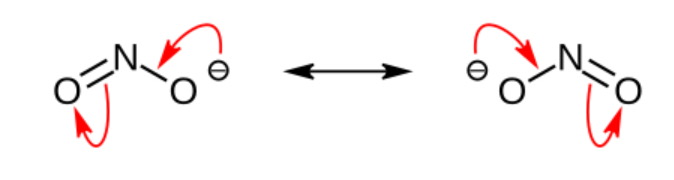
산화-환원 반응(Reaction) : 아질산염은 강한 환원제 또는 산화제로 작용할 수 있습니다. 환경에 따라 질산염(NO₃⁻)으로 산화되거나 질소 가스(N₂)로 환원될 수 있습니다.
용해도(Solubility) : 대부분의 아질산염 화합물(예: 아질산나트륨, NaNO₂)은 물에 잘 녹습니다.
- 자연에서의 존재
아질산염은 질소 순환(nitrogen cycle)의 중간 단계에서 생성됩니다. 암모니아(NH₃)가 박테리아에 의해 산화될 때 아질산염이 형성되고, 이후 질산염으로 전환됩니다.
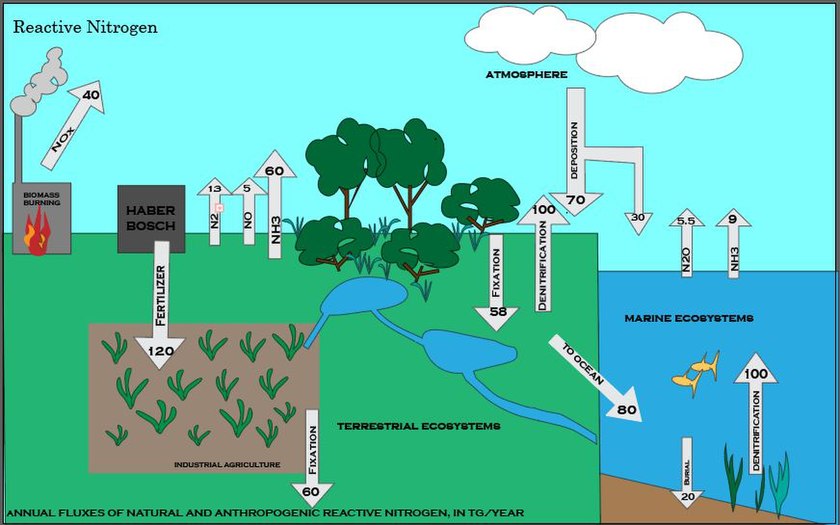
토양, 물, 생물체에서 미량으로 발견되며, 특히 질소 화합물이 분해되는 과정에서 발생합니다.
3. 용도
- 식품 : 아질산나트륨(NaNO₂)은 육류 가공(예: 햄, 소시지)에서 발색제와 보존제로 사용됩니다. 고기의 붉은색을 유지하고, 클로스트리디움 보툴리눔(보툴리즘을 일으키는 박테리아)의 성장을 억제합니다.
- 공업: 염료, 고무, 금속 가공에서 중간체로 활용됩니다.
- 의학: 과거에는 아질산염이 혈관 확장제로 사용되었으나, 현재는 주로 독성 연구나 해독제(예: 시안화물 중독 치료)로 관련됩니다.
4. 생물학적 영향과 독성
- 작용 기전: 아질산염은 혈액 내 헤모글로빈과 반응하여 메트헤모글로빈(methemoglobin)을 생성합니다. 이는 산소 운반 능력을 저하시켜 저산소증을 유발할 수 있습니다.
- 독성: 과다 섭취 시 “청색증”(methemoglobinemia)을 일으킬 수 있으며, 특히 유아에게 위험합니다(예: 오염된 물로 인한 “블루 베이비 증후군”).
- 발암성 논란: 아질산염은 위장에서 아민과 반응하여 니트로사민(nitrosamine)을 형성할 수 있는데, 이는 발암 물질로 의심받고 있습니다. 그러나 식품 내 허용량에서는 안전하다고 판단됩니다.
5. 일상생활에서 연관성
- 채소(특히 시금치, 상추)나 지하수에서 자연적으로 발생할 수 있으며, 과도한 비료 사용으로 농도가 증가할 수 있습니다.
- 식품 첨가물로 사용될 때는 엄격한 규제(예: WHO, FDA 기준)를 따릅니다.
- 최근 들어 식약처에서도 니트로사민류 불순물에 대해 1일 섭취허용량을 설정하고 시험방법을 제정하며 관리에 나서고 있습니다. 링크
6. 결론
자연에서 발생하며 여러 용도로 사용, 존재하는 아질산염에 대해 알아봤습니다. 최근 들어 니트로사민 생성으로 인한 발암성 논란으로 식약처에서도 이슈가 되고 있는데요. 다음에는 실험실에서 어떤 방법으로 아질산염을 분석할 수 있는지 시험방법을 알아보도록 하겠습니다
그림 출처 : 위키디백과